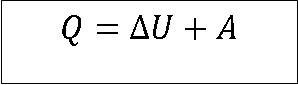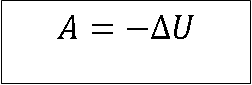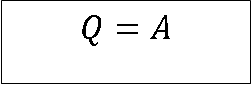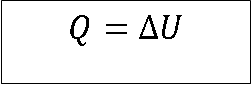Prvi princip termodinamike
Prvi princip termodinamike glasi:
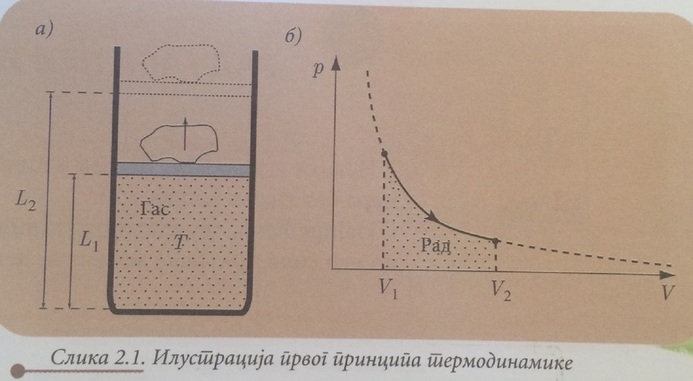
Količina toplote, dovedena izolovanom sistemu, može jednim delom da poveća njegovu unutrašnju energiju, a drugi deo može da se pretvori u rad tog sistema.
Analizom prvog principa termodinamike mogu se objasniti različite termodinamičke pojave:
- Q=0 sistem niti prima niti otpušta toplotu
Rad se vrši na račun unutrašnje energije sistema (ona se smanjuje).
Termodinamički procesi bez razmene toplote se nazivaju adijabatski procesi.
Nemoguće je konstruistati perpetuum-mobile prve vrste, tj. mašinu koja bi neprekidno vršila rad, bez utroška bilo kog oblika energije.
Termodinamički procesi bez razmene toplote se nazivaju adijabatski procesi.
Nemoguće je konstruistati perpetuum-mobile prve vrste, tj. mašinu koja bi neprekidno vršila rad, bez utroška bilo kog oblika energije.
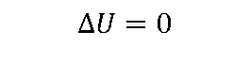
- unutrašnja energija sistema se ne menja (izotermski proces)
Dovedena količina toplote u potpunosti se troši za vršenje rada.
- A=0 sistem ne vrši nikakav rad (izohorski procesi)
Sva dovedena količina toplote troši se za povećanje unutrašnje energije sistema.